“史上最贵药”,何以卖出1465万元人民币的天价?
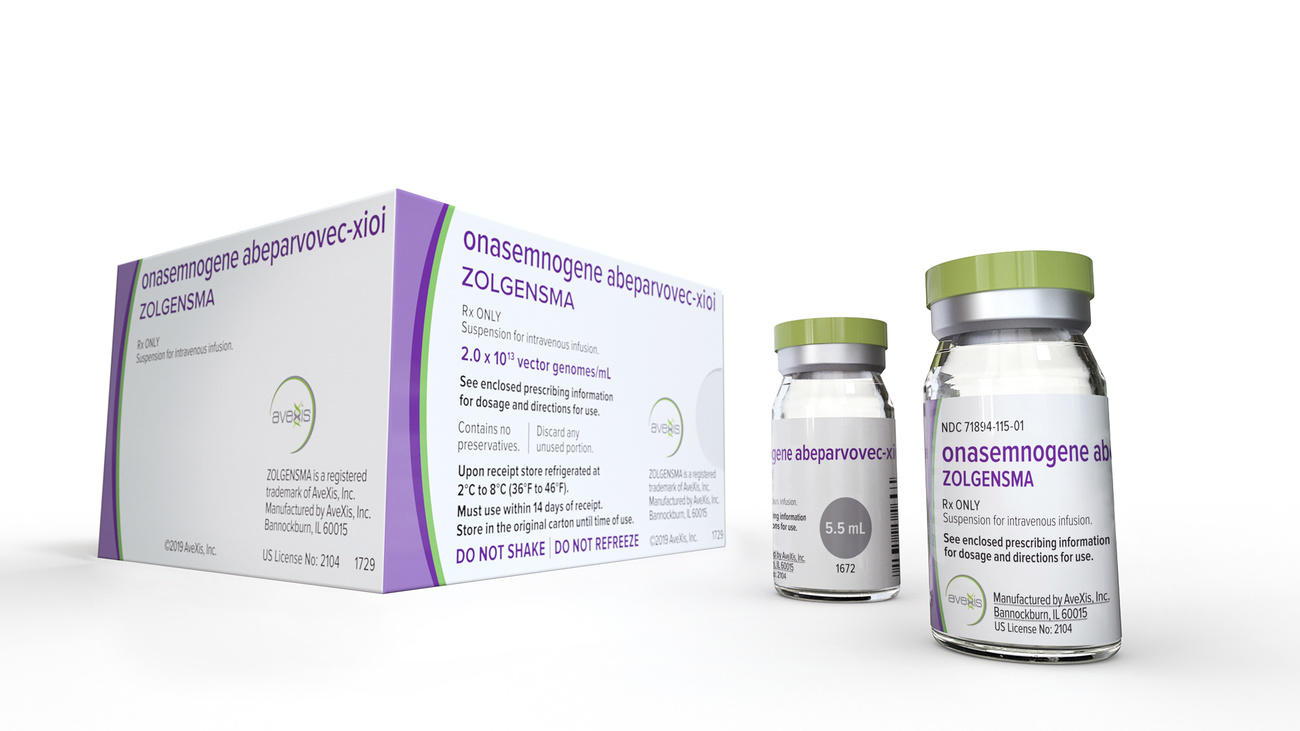
由瑞士制药巨擘诺华(Novartis)出产的用于治疗一种婴幼儿致命疾病的基因疗法,现已在美国获批上市。这款重磅新药凭借210万美元的定价,成为有史以来最昂贵的药物。近乎令人绝望的标价也招致恶评如潮。如此天价,合情合理吗?
閱讀本文繁體字版本請 點擊此處
最近在美国获批的名为Zolgensma(英)外部链接的治疗方案,属于一种基因疗法。基因疗法是一种相对较新、但正值快速上升期、发展迅猛的药物开发领域。这种疗法通过用全新的外源正常拷贝基因导入靶细胞,置换或补偿原有的致病缺陷基因,从而达到治疗目的。从某种意义上来说,这些治疗方案并非单纯治标,而是着眼于解决病症的根源-即有缺陷的基因,这种做法能消除众多儿童致命疾病、多种罕见血液疾病以及遗传性癌症。
基因疗法Zolgensma用于治疗被称为婴幼儿“头号遗传病杀手”的小儿脊髓性肌肉萎缩症(SMA,英)外部链接。这是一种因基因缺陷所导致的常染色体隐性遗传致命疾病,会导致婴幼儿肌肉张力显著低下,肌肉呈现严重无力,随着病情恶化,他们逐渐丧失移动能力,并最终会出现吞咽或呼吸功能障碍。急性婴儿起病的小儿脊髓性肌肉萎缩症患者,通常会在年满两岁之前便早早夭折。大约1万名左右的新生儿中,就有一位会饱受这种致命疾病之苦,这种病也因此成为较为常见的罕见病之一。
基因疗法Zolgensma是美国食品和药物管理局(FDA)截至目前批准的第17种细胞和基因疗法(英)外部链接。不过据该机构预计,截至2025年,每年获批、从而大规模上市的细胞和基因疗法有望多达10到20种。目前,遍布38个国家的2600例左右的基因治疗临床试验(英)外部链接,部分尚在进行中,部分则业已完成。
总部位于瑞士的制药及生物技术跨国企业诺华(Novartis)和罗氏(Roche),当属基因治疗革命时代的弄潮儿,而近期,这两家制药巨擘相继收购(英)了数家规模相对较小的生物科技公司。
基因疗法Zolgensma并不是唯一因其惊世骇俗的高昂售价而引发质疑的治疗方案。数年前,继一种标价高达6万美元(折合人民币约为42万元)、用于治疗丙型肝炎的药物上市之后,瑞士各界激辩(英)便接踵而至,经久不息。
在美国消费者新闻与商业频道(commentary)的评论节目中(英)外部链接,诺华集团首席执行官瓦斯·纳西姆汗(Vas Narasimhan)辩驳道,基因疗法通过单剂量一次性注射药物,为治愈致命的遗传性疾病提供了希望,从而象征着医学领域的重大突破。在有些病例中,备选的可供替代方案,是渐进式增量的多剂量递增疗法。
基因疗法Zolgensma是适用于两岁以内婴幼儿的一次性注射药物,注射持续时长大约需要一个小时。与此同时,罗氏制药也在针对小儿脊髓性肌肉萎缩症积极研发一款口服溶液。
对患者来说,另一种选择是同样用于治疗孩童及成人遗传性脊髓性肌肉萎缩症、且早于2016年便通过美国食品和药物管理局批准的Spinraza。该药物需按照一年四次的频率终身服用。第一年的定价为75万美元(约合人民币520万元),此后每年需花费35万美元(折合人民币约为242万元),这意味着服药10年共耗资约400万美元(约合人民币2770万元)。
负责对价格昂贵的新药的价值与裨益(英)外部链接进行评定的独立非营利机构-临床与经济审核研究所(Institute for Clinical and Economic Review)通过计算得出结论,这种全新基因疗法(英)外部链接成本就高达120万至210万美元,且正因为它“显著改变了遭受这种毁灭性疾病影响的家庭的生活和命运”,因此,其定价是正当合理、无可非议的。
确实存在数个争议焦点。首先是该药物定价究竟是如何确定的,以及不同的利益相关体利润空间具体几何-尤其是在目前外界对此类基因治疗药物所耗成本知之甚少的情况下。实际上,诺华并非基因疗法Zolgensma的研发方,它是通过以870万美元的收购价(英)外部链接将美国基因治疗公司AveXis收入囊中、从而获得了该公司最先进的基因疗法Zolgensma。
除此之外,不少企业坚持主张,药品价格是基于其价值的定价决策模型而最终计算得出的,但这种药物定价模型会引发诸多令人焦头烂额的问题。不仅如此,围绕这些基因疗法到底是否有效、会不会伴随潜在风险-尤其是从长期治疗来看,截至目前也缺乏相应的证据。现有市场上的某些疗法,譬如用于治疗皮肤及淋巴结黑色素瘤病变的Imlygic(英),并未真正发挥效用。
许多基因疗法的确能够治愈罕见病,从而为显著改善罕见病患者的生活境遇提供了新的可能性,然而这一事实却让人们对基因疗法的认知和评判变得更为不明朗。甚至有批评(英)外部链接指出,这会驱使(制药企业)将关注焦点不再放在糖尿病和高血压等常见疾病上。
此外,与操纵基因相关的一系列伦理议题(英)外部链接、以及对走向基因编辑“定制婴儿”(英外部链接)的失控式滑坡的恐惧,也始终存在。
然而最终,争议的根源在于社会该如何为这些昂贵的基因疗法“买单”。绝大多数现行的医疗保险制度从架构设计上并不适用于耗资如此高昂的一次性治疗。诺华业已表示,其目前正与多家保险公司携手合作(英),以便让患者通过5年分期、平均每年花费42.5万美元的方式来支付药物费用;倘若治疗无效,会退还部分付款。但这项举措具体在不同的国家会如何实施,尚属未知。

符合JTI标准



您可以在这里找到读者与我们记者团队正在讨论交流的话题。
请加入我们!如果您想就本文涉及的话题展开新的讨论,或者想向我们反映您发现的事实错误,请发邮件给我们:chinese@swissinfo.ch。