Le scandale des implants mammaires arrive en Suisse
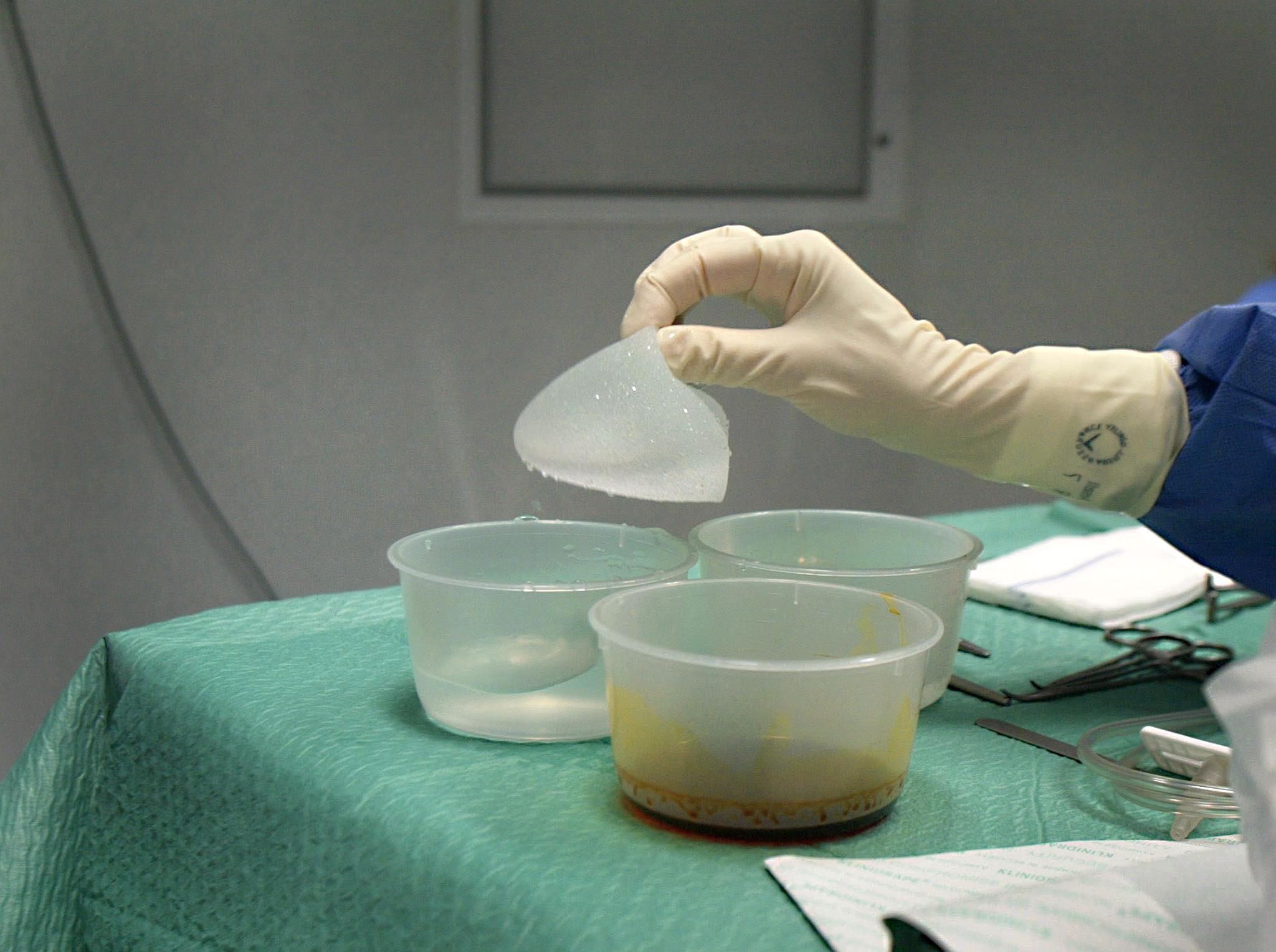
La France recommande aux femmes porteuses d’implants PIP de les retirer. Les autorités sanitaires suisses se montrent plus prudentes et disent attendre les recommandations de Bruxelles. Mais à Genève, un groupe de femmes a déposé plainte contre le fabricant français.
Contrairement aux autorités françaises, l’Institut suisse des produits thérapeutiques (Swissmedic) ne recommande pas le retrait préventif systématique des prothèses produites par la société Poly Implant Prothèse (PIP). Une décision âprement contestée par une nouvelle association créée il y a quelques jours à Genève.
Dénommée «Victimes du 95 C» (en référence à la taille du bonnet du soutien-gorge), l’association a demandé au procureur général de Genève d’ouvrir une procédure pénale contre la société PIP pour avoir vendu «des prothèses mammaires frauduleuses» en Suisse.
Près de 300’000 femmes du monde entier se sont fait implanter des prothèses mammaires PIP avant que la société ne fasse faillite en 2010. Une enquête officielle a révélé que la firme française utilisait du silicone non conforme aux normes et non approuvé par les autorités compétentes dans une partie de ses produits.
Les vérifications entreprises en France ont démontré que les implants mammaires présentaient un risque élevé de rupture. Paris a ainsi conseillé à 30’000 femmes porteuses de telles prothèses de se les faire enlever à titre préventif. En Europe, la même recommandation a été formulée par les autorités sanitaires allemandes, hollandaises et tchèques.
Peu de Suissesses concernées
De son côté, Swissmedic motive son approche prudente par le fait qu’à l’heure actuelle, aucune preuve scientifique d’une augmentation du risque de cancer du sein n’a été apportée. L’Institut relève d’autre part que le nombre de femmes – environ 280 – qui sont porteuses de tels implants en Suisse est extrêmement faible.
L’association «Victimes du 95 C» ne partage pas du tout le point de vue de Swissmedic. Dans sa lettre envoyée au procureur général de Genève, l’association souligne qu’en utilisant un gel bon marché et de mauvaise qualité pour ses prothèses, la société française a mis en danger la vie des femmes implantées.
L’association reproche à la Suisse de ne pas en faire assez: «C’est comme si ce scandale de santé publique, qui préoccupe le reste de l’Europe, s’était arrêté à la frontière», s’insurge la députée communale genevoise Salika Wenger, fondatrice de «victimes du 95 C». L’association a demandé au procureur de Genève d’interdire toute utilisation des prothèses mammaires controversées et d’en ordonner le séquestre.
Des femmes furieuses
«La position de Swissmedic, selon qui ce problème n’est pas très important et n’affecte que peu de monde, a rendu furieuses toutes les femmes confrontées à de réels problèmes», explique Salika Wenger. La députée d’extrême gauche affirme avoir connaissance du cas d’une femme dont les implants se sont rompus et le liquide répandu dans son corps.
«Nous ne sommes pas nombreuses, à peine une douzaine. Mais depuis que nous avons fondé l’association, de nombreuses personnes m’ont téléphoné ou envoyé des e-mails pour me faire part de leurs problèmes et de leur désir de rejoindre l’association», relève Salika Wenger.
«Nous estimons que Swissmedic, qui a le devoir de contrôler si un produit peut être mis ou non sur le marché, n’a pas fait son travail. Nous pensons que les autorités publiques, notamment le gouvernement, ne prennent pas au sérieux leur travail», ajoute la députée.
Autorisés par l’UE
Swissmedic est en premier lieu responsable de l’homologation et de la surveillance des médicaments. Le contrôle de qualité des implants médicaux entre dans le champ des relations bilatérales de la Suisse avec l’Europe. Elle est ainsi soumise aux procédures européennes.
Les implants PIP ont été autorisés en Europe par un organisme de réglementation en Allemagne, lequel a octroyé le «label UE». Cette certification garantit la compatibilité avec les normes sanitaires et de sécurité établies par la Commission européenne. Une fois que le produit a obtenu le «label UE», il peut être distribué en Europe sans la nécessité de vérifications ultérieures. Ce système a déjà été critiqué par les médecins dans un passé récent.
«Swissmedic ne contrôle pas à nouveau ces produits, confirme le porte-parole de Swissmedic Daniel Lüthi. Une fois que l’organe de notification donne son feu vert, les médecins sont autorisés à acquérir ce produit et à l’utiliser». Swissmedic intervient si les produits sont défectueux. Par exemple, dans le cas des prothèses PIP, pour informer les patients concernés. «Les hôpitaux qui utilisent le produit doivent vérifier s’il y a de mauvaises expériences, fuites ou incidents, et doivent nous en faire part le cas échéant. Ensuite, nous échangeons cette information avec d’autres autorités compétentes», détaille Daniel Lüthi.
L’UE veut serrer la vis
Dans le système actuel, une grande part de la responsabilité repose sur les épaules du médecin, affirme Daniel Lüthi. A la lumière du scandale des prothèses mammaires PIP, le système européen pourrait être modifié. Début janvier, le nouveau directeur exécutif de l’Agence européenne des médicaments Guido Rasi a souligné la nécessité de renforcer les normes sur les dispositifs et le matériel médical.
«Je vois un besoin urgent d’adopter les mêmes mesures de sécurité pour le matériel médical que pour les médicaments», a déclaré Guido Rasi à l’agence de presse Reuters. D’après lui, la peur des prothèses mammaires PIP pourrait accélérer les changements dans le secteur des technologies médicales.
De nouvelles propositions émanant de la Commission européenne devraient être proposées cette année aux ministres de la santé des 27 pays de l’UE. Elles comprennent notamment un nombre plus important de contrôles avant la mise sur le marché du matériel médical et une surveillance accrue une fois dans le commerce.
La Suisse suivra l’UE
Si ces propositions étaient adoptées, la Suisse suivrait l’exemple, indique Swissmedic: «Si l’Europe décide de changer quelque chose dans ces recommandations, nous n’avons naturellement aucun motif de ne pas la suivre, car nous faisons partie du réseau international», souligne Daniel Lüthi.
Entretemps, Swissmedic a continué à suivre le dossier avec ses homologues des autres pays et à échanger les données les plus récentes. Mais au final, aucun motif n’a poussé les responsables à modifier les directives. Le porte-parole précise que Swissmedic examinera ultérieurement la situation si d’autres «signaux, preuves médicales ou résultats scientifiques» des effets négatifs des implants PIP défectueux devaient être constatés.
D’ici là, les lignes directrices de l’Institut publiées en décembre, qui préconisent aux femmes implantées de se soumettre à des contrôles réguliers tous les six mois, restent valides. Et en cas de problème, elles doivent consulter immédiatement un médecin.
Durant des années, la société française PIP (Poly Implant Prothèse) a utilisé du silicone industriel de mauvaise qualité, fabriqué à bas coût et non certifié, pour produire des prothèses mammaires. En mars 2010, l’agence de vigilance sanitaire française a découvert que les prothèses PIP avaient un taux de rupture nettement plus élevé que la moyenne.
L’enquête qui a suivi a démontré que PIP utilisait un silicone à usage industriel et non à usage médical. En avril 2010, le produit a donc été retiré du marché et la société a été fermée. Plus de 80% des prothèses fabriquées par PIP ont été exportées, la majorité en Europe et en Amérique latine.
Le fondateur de la société, Jean-Claus Mas, a admis avoir utilisé le silicone non conforme dans trois quarts des prothèses. En France, le taux de rupture des prothèses PIP a atteint 5%, contre 1% pour les autres fabricants. Une proportion qui n’a toutefois pas été confirmée dans les autres pays.
Lorsqu’une prothèse se rompt, le gel peut se répandre dans le corps. Si le risque accru de cancer n’est pas établi, le gel peut provoquer des inflammations douloureuses au sein qui rendent nécessaire son explantation. L’opération peut se révéler plus délicate lorsque la prothèse est rompue.
Les autorités sanitaires nationales ont formulé des conseils différents aux porteuses des prothèses PIP. La France, la République tchèque, l’Allemagne, les Pays-Bas et le Venezuela ont recommandé le retrait par précaution. Mais d’autres pays, parmi lesquels la Suisse et la Grande-Bretagne, ont déclaré que c’était probablement inutile, précisant que l’explantation est une opération et qu’elle peut aussi représenter un risque.
(Adaptation de l’anglais: Samuel Jaberg)

En conformité avec les normes du JTI
Plus: SWI swissinfo.ch certifiée par la Journalism Trust Initiative




Vous pouvez trouver un aperçu des conversations en cours avec nos journalistes ici. Rejoignez-nous !
Si vous souhaitez entamer une conversation sur un sujet abordé dans cet article ou si vous voulez signaler des erreurs factuelles, envoyez-nous un courriel à french@swissinfo.ch.