Du laboratoire au patient, un parcours du combattant
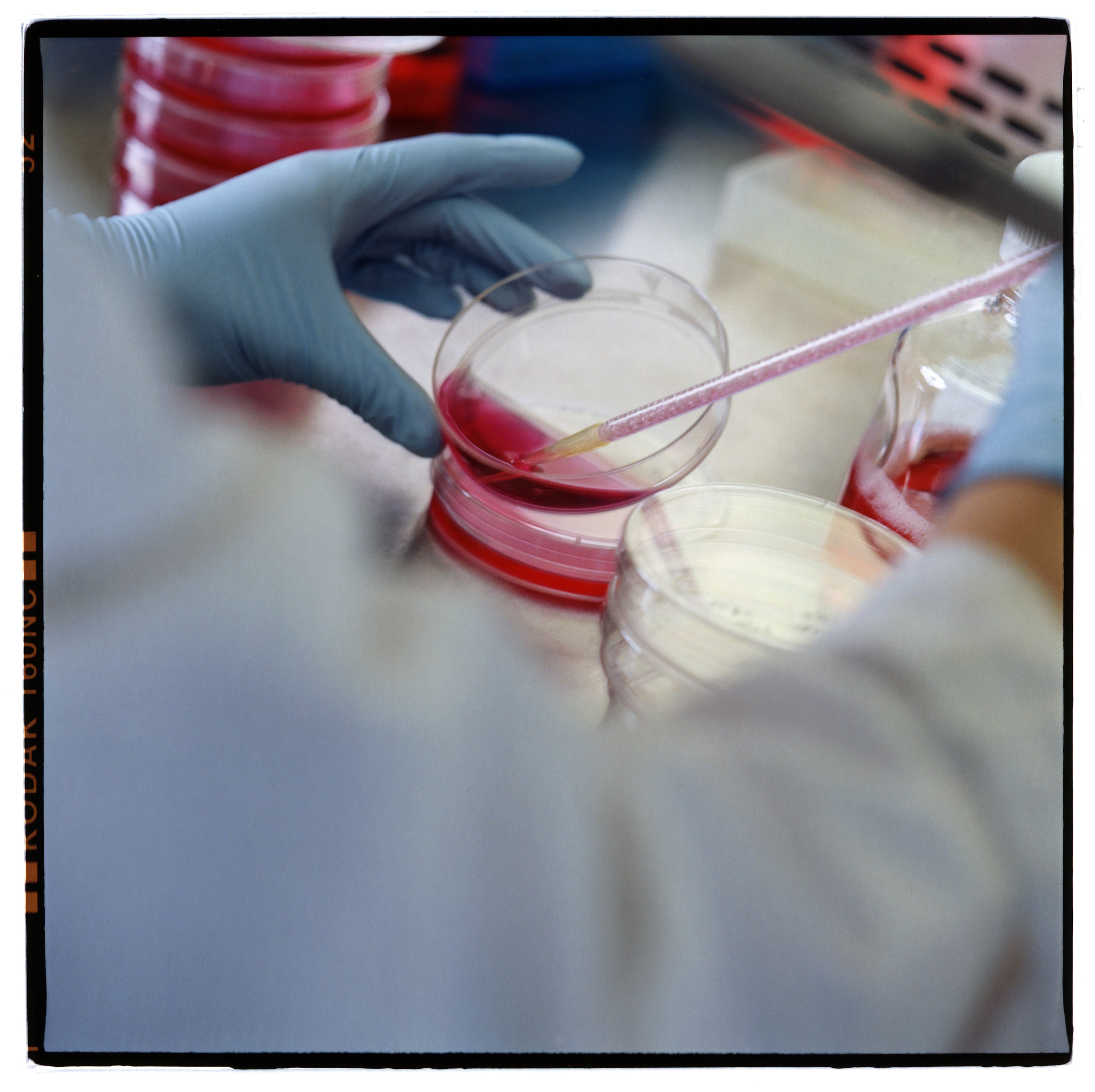
Le processus menant de la découverte d’un médicament à sa mise sur le marché est onéreux et peut parfois durer près de 30 ans. Les embûches ont encore augmenté ces dernières années, se plaignent l’industrie pharmaceutique et les instituts de recherche suisses.
Les autorités sanitaires sont non seulement devenues plus prudentes et restrictives, mais elles exigent de plus en plus de documentation, affirme Stefan Frings, responsable de la division oncologie au sein de l’organisation partenaire de Roche qui achète des médicaments pour leur développement ultérieur.
Il y a quelques décennies, une thérapie aurait été approuvée pour n’importe quel type de tumeur sur la base de données relativement limitées, explique Stefan Frings. Aujourd’hui, les médicaments sont uniquement enregistrés pour les types de tumeur pour lesquels ils ont été étudiés. Avec cette approche, les régulateurs veulent non seulement s’assurer que les médicaments sont sûrs et efficaces mais également qu’ils apportent une amélioration par rapport aux traitements existants.
Décrocher l’autorisation de vendre un médicament par Swissimedic ou une autre instance d’homologation ne représente pourtant qu’un des nombreux obstacles à franchir. Les entreprises doivent également négocier les prix avec les agences gouvernementales qui décident de leur remboursement – en Suisse, l’Office fédéral de la santé publique (OFSP). Et les gouvernements sont de plus en plus réticents à payer pour des traitements onéreux.

Plus
A la pointe des traitements contre la leucémie
Jusqu’à 2 milliards de francs
En Suisse, le coût-efficience ou coût-bénéfice d’un médicament est déterminé sur la base de comparaisons avec d’autres thérapies et évaluations qui sont réalisées dans d’autres pays, affirme Daniel Dauwalder, porte-parole de l’Office fédéral de la santé publique (OFSP).
«Même si nous parvenons à obtenir l’homologation, cela ne signifie pas pour autant que nous soyons autorisés à délivrer le médicament aux patients, affirme Stefan Frings. Dans la plupart des pays, nous avons à subir un nouvel examen, sous la forme d’un ‘value dossier’ [un dossier qui rassemble toutes les preuves scientifiques et économiques pertinentes pour soutenir la valeur d’un médicament]».
Tous ces obstacles s’additionnent à un processus déjà long et laborieux. Le Tufts Center for the Study of Drug Development de Boston estime qu’un nouveau médicament n’a qu’une chance sur 5000 d’arriver un jour sur le marché. Selon une étude publiée en 2006, son coût total de développement oscille ainsi entre 500 millions et 2 milliards de dollars.
Sur 5000 médicaments potentiels, seul un parvient finalement sur le marché. Sur 5000 à 10’000 candidats, 250 sont suffisamment prometteurs pour être évalués en laboratoire et testés sur les animaux. Environ 10 d’entre eux seront ensuite testés sur les humains.
Selon le Tuffs Center for the Study of Drug Development de Boston, seul un médicament sur cinq qui entre dans le processus des essais cliniques recevra l’homologation pour sa commercialisation.
Cinq ans, un record
La première étape dans la découverte de traitements contre le cancer consiste à étudier comment les cellules cancéreuses envahissent le corps humain. Mieux l’on connait la maladie, plus rapidement il est possible de développer une thérapie et d’identifier les patients qui pourraient en bénéficier, souligne Stefan Frings. Certaines molécules sont déjà prometteuses à des stades précoces du développement de la maladie.
«Avec le Zelboraf [un médicament contre le cancer de la peau commercialisé aux Etats-Unis et en Europe] nous avons su dès la première étape que nous tenions là un médicament. Il n’a fallu que cinq ans pour qu’il obtienne le feu vert des autorités aux Etats-Unis».
Ce cas, chanceux, est cependant plutôt rare. Le développement des médicaments prend généralement entre 5 et 30 ans, 10 en moyenne, selon le représentant de Roche. Le Perjeta, un anti-cancéreux du sein commercialisé par Roche, a reçu l’approbation des autorités européennes au début de cette année, soit un quart de siècle après la découverte scientifique fondamentale à la base du traitement.
«Si vous n’êtes pas capable de soutenir des efforts de recherche et de développement prolongés, qui durent parfois 10 ou 20 ans, vous vous retrouvez tôt ou tard écarté du business», ajoute le spécialiste de Roche.
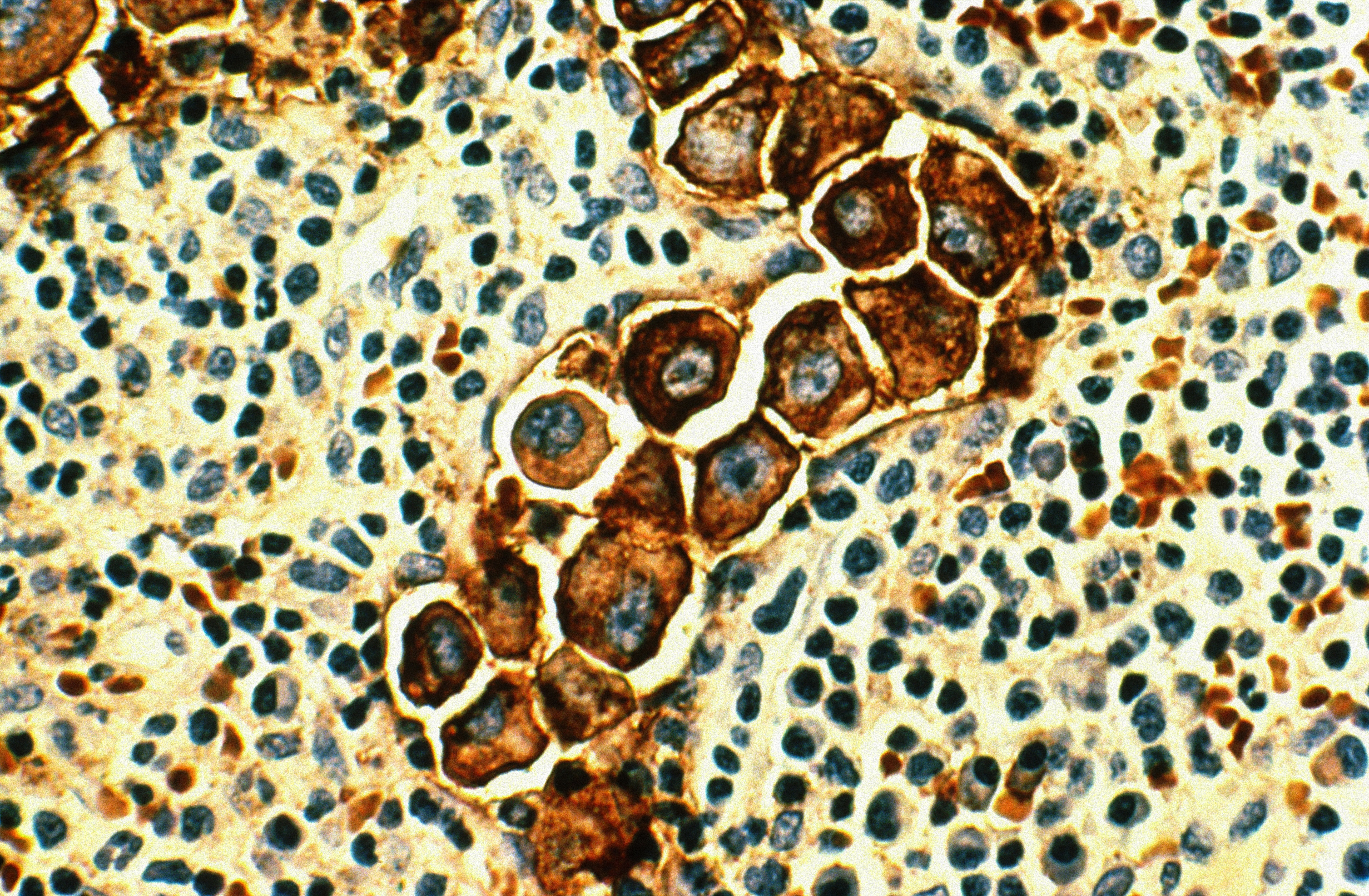
Plus
La recherche sur le cancer, toujours une bonne affaire?
La Suisse investira davantage
De nombreux médicaments contre le cancer développés avec succès sont le résultat de recherches sur les mécanismes de la maladie menés par des universités ou des instituts de recherche des années auparavant. Ces projets dits de recherche fondamentale sont généralement financés par des fondations de droit privé comme la Recherche suisse contre le cancer (RSC) ou le Fonds national suisse (FNS).
Le FNS, qui dispose d’un budget annuel de l’ordre de 700 millions de francs, est la plus importante institution suisse de promotion de la recherche scientifique fondamentale. Entre 2008 et 2012, elle a attribué plus de 100 millions de francs à des projets liés à la recherche sur le cancer, une manne qui devrait encore croître à l’avenir, affirme son porte-parole Ori Schipper.
Le FNS investit par exemple dans des projets visant à mieux comprendre les mécanismes biologiques des cellules cancéreuses. Des découvertes qui ne mèneront pas nécessairement à une application pratique dans les 20 prochaines années, souligne Sabine Werner, spécialiste en biologie cellulaire à l’Ecole polytechnique fédérale de Zurich (EPFZ).
La Suisse dépense environ 2,3 % de son Produit intérieur brut (BIP) pour la recherche et le développement, se classant au 11e rang mondial. Les entreprises actives dans l’industrie pharmaceutique et chimique contribuent aux trois-quarts de ces dépenses, le quart restant provenant du secteur public.
Mutations génétiques
Les découvertes scientifiques fondamentales ne sont souvent appliquées que bien plus tard dans le processus de développement des médicaments. Certaines découvertes des années 1990 contribuent encore aujourd’hui au développement de nouveaux médicaments, affirme Stefan Frings.
«Nous n’en serions pas là si nous n’avions pas mené certaines recherches en matière de mutations génétiques il y a 20 ans dont nous savons aujourd’hui qu’elles jouent un rôle dans le cancer du sein», relève Sabine Werner. La représentante du FNS fait référence à l’Herceptin, le troisième médicament le plus vendu au monde. Il est utilisé pour traiter le cancer du sein métastasique HER2 positif.
Une telle découverte n’est cependant qu’un premier pas. Dans un deuxième temps, les petites entreprises de biotechnologie testent et analysent les molécules prometteuses. Celles qui restent en course sont ensuite vendues à des fabricants de médicaments tels que Roche et Novartis.
De nombreux spécialistes affirment que la meilleure manière d’accélérer le processus menant du développement d’un médicament du laboratoire au chevet du malade est de mettre sous un même toit scientifiques et praticiens.
C’est ce que prévoit le centre de cancérologie AGORA de Lausanne, qui doit ouvrir ses portes en 2016 à Lausanne. Le projet a été initié par l’Ecole polytechnique fédérale de Lausane (EPFL), la fondation ISREC et des oncologues de l’Hôpital universitaire de Lausanne (CHUV).
«La Suisse peu attractive»
Les développeurs de médicaments testent ces nouvelles substances chimiques en laboratoire et, finalement, sur les humains, évaluant d’abord leur sécurité puis leur efficacité. Lors d’une troisième et dernière phase précédent l’homologation, les médicaments en lice sont comparés aux traitements existants les plus couramment utilisés. Ces tests finaux sont destinés à convaincre les autorités du bienfait du médicament en vue de sa commercialisation.
Mais de telles exigences réglementaires ne sont pas seulement un obstacle pour des entreprises qui souhaitent commercialiser un produit. Les instituts de recherche sont également engagés dans cette bataille de tous les instants. Selon le Groupe suisse de recherche clinique sur le cancer (SAKK), le nombre de tests cliniques approuvés par Swissmedic a diminué de 40% entre 2005 et 2011.
«La raison de cette baisse est la sur-réglementation, qui rend la Suisse peu attractive, car le processus y est dispendieux et lent, affirme Beat Thürlimann, président du groupe. Il est ainsi plus compliqué de mener de tels tests cliniques aujourd’hui».
Pourtant, pour un oncologue comme Beat Thürlimann, il est plus urgent que jamais de trouver de meilleures thérapies contre le cancer. Près de 40’000 nouveaux cas sont traités chaque année en Suisse, qui sont responsables de la mort de près de 16’000 personnes, d’après la Ligue suisse contre le cancer.
Swissmedic, par l’intermédiaire de son porte-parole Daniel Lüthi, affirme pourtant que le cadre législatif est resté le même. Il concède toutefois que l’état des connaissances scientifiques et techniques et les exigences réglementaires qui en découlent – notamment en ce qui concerne les tests cliniques et leur évaluation – a «énormément évolué» au cours des 20 dernières années.
(Traduction de l’anglais: Samuel Jaberg)

En conformité avec les normes du JTI
Plus: SWI swissinfo.ch certifiée par la Journalism Trust Initiative



Vous pouvez trouver un aperçu des conversations en cours avec nos journalistes ici. Rejoignez-nous !
Si vous souhaitez entamer une conversation sur un sujet abordé dans cet article ou si vous voulez signaler des erreurs factuelles, envoyez-nous un courriel à french@swissinfo.ch.