
Как искусственный интеллект помогает создавать вакцины
Как же это вдруг «злым концернам» удалось в рекордные сроки разработать вакцину от Ковид, ведь раньше на это уходили годы?
Русскоязычная версия: Нина Шулякова
На данный момент в Швейцарии официальный допуск получили уже две высокоэффективные вакцины против COVID-19. Столь быстрая разработка столь сложных препаратов стала возможной благодаря технологиям искусственного интеллекта, отказа от лишней бюрократии, а также в условиях развития и внедрения инновационных форм сотрудничеств ученых и экспертов из самых разных стран мира, включая и Швейцарию.
Искусственный интеллект (ИИ) ставит нас перед сложными этическими проблемами. При этом не подлежит сомнению тот факт, что самообучающиеся сети способны уже скоро совершить очередную революцию в науке и, в частности, решить некоторые из самых сложных проблем, с которыми сталкивается сейчас, например современная биология. Среди них -уж5ндх саэ предсказание структуры неизвестных нам ранее новых белков. Такого рода знание поможет проникнуть в секреты строения клеток человеческого организма и начать более эффективно противодействовать заболеваниям, непосредственно влияющим на их «здоровье».
Однако в последнее время если проблемы структуры белков и оказалась в центре внимания учёных и даже в целом мирового сообщества, то только потому, что эти и иные релевантные вопросы играют ключевую роль в быстрой разработке качественных новых вакцин, в данном случае вакцин против COVID-19. Речь идет, например, об использовании т.н. матричной (информационной) рибонуклеиновой кислоты (РНК), помогающей, не меняя ДНК человека, вооружать его иммунную систему способностью противостоять коронавирусной напасти.

Показать больше
Должны ли роботы платить налоги?
Но как же так? — спросят нас корона-скептики. Экспериментальное моделирование структуры белка — это долгий и страшно трудоёмкий процесс! На него обычно уходят месяцы исследований и тратятся серьёзные ресурсы. Как же это вдруг «злым концернам» удалось в рекордные сроки разработать новую вакцину? Не иначе как Билл Гейтс лично намешал тут «спирт с водой». В самом деле, информация о структуре белка важна как для изучения новых вирусов, так и понимания схемы их поведения и разработки эффективных вакцин. А быстро? Дело в том, что в последнее время наука и экономика имеют доступ к качественно иным вычислительным компьютерным мощностям.

Показать больше
Робот вместо трактора в полях Швейцарии?
Чудеса, которые на глазах всего мира творит Илон Маск, связаны не в последнюю очередь именно с использованием новых компьютерных технологий и в том числе — так называемого искусственного интеллекта. Ведь что такое ИИ? Упрощенно говоря, это есть не что иное, как новый уровень методов обработки того, что еще недавно называлось «большие объемы данных» (big data). Такие методы позволяют теперь не только сажать обратно на землю отработанные разгонные ступени ракет, качественно снижая стоимость полетов в космос, но и предсказывать, как будет выглядеть структура неизвестных ранее искусственно синтезированных белков. Как видим, эти методы, ставшие совсем недавно доступными для инженеров и учёных, значительно ускоряют процессы НИОКР и в невиданной степени повышают точность их результатов.
Благодаря новейшим достижениям в области искусственного интеллекта теперь можно с высокой точностью предсказать, как будут выглядеть трёхмерные структуры даже самых сложных протеинов, синтезированных специально для решения той или иной задачи. Важной вехой на этом пути стал тот момент, когда система искусственного интеллекта AlphaFold2Внешняя ссылка, созданная лондонской компанией DeepMind (с 2014 года принадлежит Google), позволила быстро идентифицировать несколько белковых структур вируса SARS-CoV-2, о котором мы ещё несколько месяцев назад не знали практически ничего.
Качественный скачок в науке
Именно «авральная» работа учёных и эффективное международное сотрудничество на основе передовых технологий искусственного интеллекта, таких как разработки компании DeepMind, и позволили оперативно отреагировать на пандемию созданием новых вакцин. По данным Всемирной организации здравоохранения (ВОЗ), в настоящее время на различных стадиях клинических испытаний находятся около 60 видов вакцин, а три вакцины уже были одобрены для широкого использования надзорными органами ряда стран, включая Швейцарию.
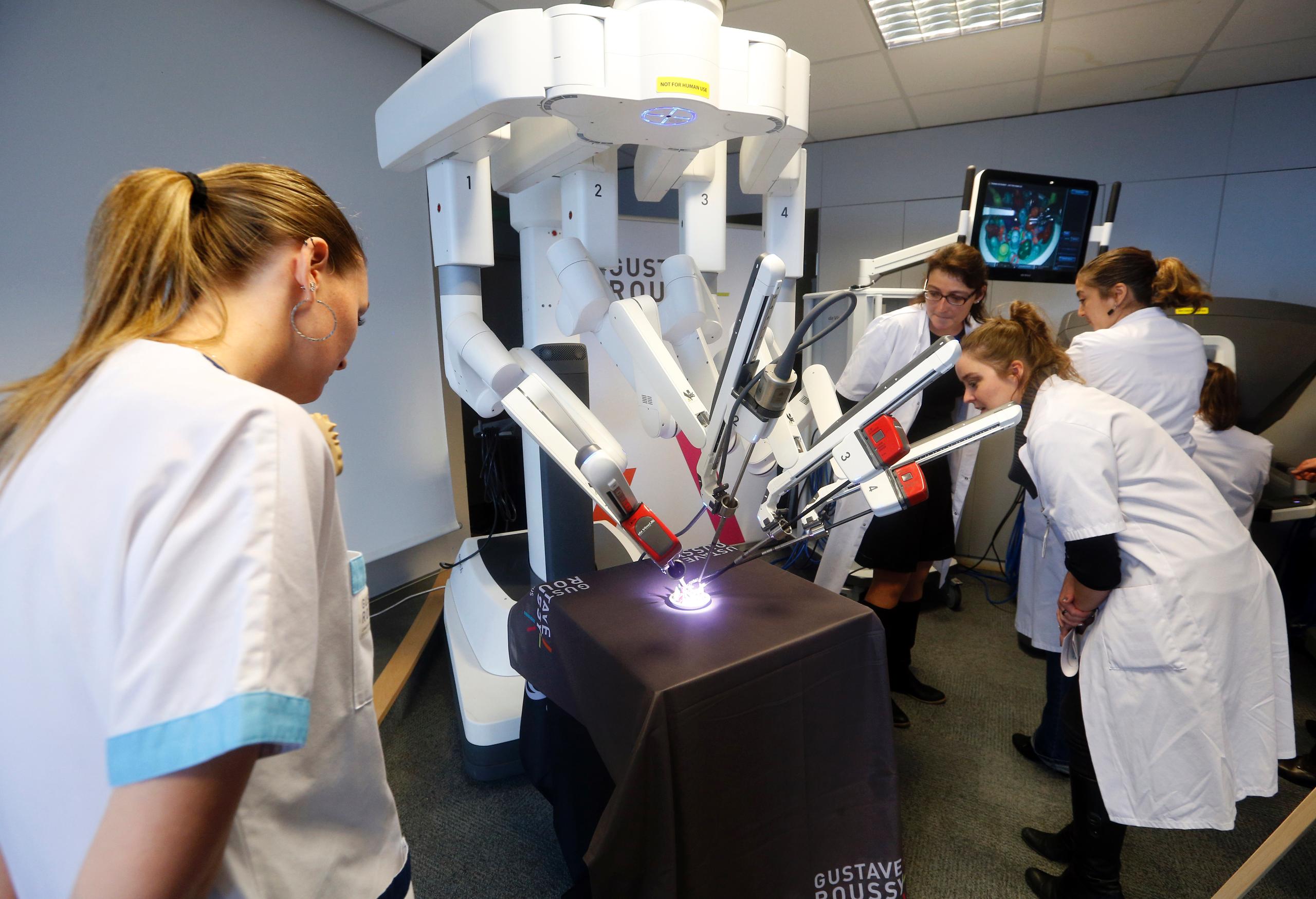
Показать больше
Как в Женеве роботы помогают хирургам
Здесь на момент создания данного материала сертификаты и допуски получили уже две вакцины. Эксперты-биомедики считают, что именно этот момент и стал настоящим поворотным пунктом в науке. «Это совершенно невероятное достижение», — говорит Торстен Шведе (Torsten Schwede), проректор по научной работе Базельского университета и руководитель целевой экспертной группы в Швейцарском институте биоинформатики (Forschungsgruppe am Schweizerischen Institut für Bioinformatik SIBВнешняя ссылка).
Под его руководством тут был разработан SWISS-MODELВнешняя ссылка, полностью автоматизированный сетевой сервер, дающий возможность моделировать структуры белков ученым из какой угодно страны мира. Без проекта SWISS-MODEL не были бы возможны и нынешние достижения компании DeepMind, достигнутые ею в области вычислительной структурной биологии. Но еще раз: почему же в последнее время белки и протеины стали объектом столь пристального внимания медиков и учёных?
Люди и программы
Протеины, может быть, и не видны невооруженным глазом, но жизненно важны, так как именно они лежат в основе базовых химических и биологических процессов жизнедеятельности клеток любого живого организма, включая человеческий. Аминокислоты, входящие в их состав, вступают в связь друг с другом, спонтанно образуя трёхмерные модели, аналогичные оригами. Эти «оригами» и составляют уникальную структуру белков.

Показать больше
Как цифровая революция влияет на занятость?
Способность предсказывать их точную форму смогла бы значительно ускорить важные исследования в области биомедицины, например, сделав огромный шаг в изучении болезней человека. Благодаря этим знаниям научное сообщество уже сейчас получает все больше возможностей в плане разработки новых лекарств и передовых методов терапии. SWISS-MODEL стал первой в мире автоматизированной компьютерной системой в режиме онлайн, способной автономно моделировать трёхмерную структуру белков, не исследованных экспериментально в лаборатории.
Идею использования компьютерного моделирования, которое, не требуя вмешательства человека, позволило бы получать информацию о структуре белков с целью качественно лучшего понимания их важнейших молекулярных функций, еще в 1993 году выдвинул Мануэль Пайч (Manuel PeitschВнешняя ссылка), специалист в области биоинформатики и создатель сервера SWISS-MODEL. Тогда этот проект показался просто какой-то научной фантастикой, равно как и проект посадки ракеты на плавающую посреди океана платформу. Сегодня благодаря всё более эффективным вычислительным алгоритмам, качественно превзошедшим человеческие возможности, все эти проекты стали реальностью.
В области биотехнологий, в частности, они позволяют сравнивать уже известные белковые структуры с генными последовательностями еще неизвестных, но в теории возможных белков. Речь идет при этом о так называемом «гомологическом моделировании». Ежегодно сервер SWISS-MODEL обрабатывает более миллиона запросов на моделирование структур белков, и все это без участия человека, автономно. Проблема только в том, что белки (или протеины) — это очень гибкие объекты, которым для полноценного функционирования необходимо вечное движение, своего рода «статическое мерцание».

Показать больше
Роботы помогут преодолеть спад в швейцарской промышленности
Для сравнения трёхмерной модели имеющегося белка с экспериментальной структурой необходимо «разворачивать» их друг относительно друга до тех пор, пока между ними не возникнет наибольшая степень совпадения. Но для гибких объектов, постоянно «вибрирующих» и изгибающихся, такой позиции добиться очень сложно. Решая эту проблему, команда SWISS-MODEL разработала программу под названием Local Distance Difference Test («Тест локальной разницы расстояний», или LDDTВнешняя ссылка).
Этот показатель оценивает и предсказывает, в какой степени фактическая структура нового белка будет совпадать с оригинальной моделью, независимо от любых внутренних интрамолекулярных вибраций. Получаемый без участия человека в самом процессе вычисления, он жизненно необходим для разработки методов автономного моделирования белков.
Реальность и научная фантастика
В течение последних трёх десятилетий учёные пытались выделять характерные трёхмерные структуры белков из их аминокислотных последовательностей. Понимание того, как выглядят экспериментальные структуры родственных белков, делает такое моделирование относительно простым и точным. Но в сложных случаях отсутствие информации о структуре определенного семейства белков означает, что очень сложные и часто неточные прогнозы приходится делать с нуля. Благодаря технологии AlphaFold2 это обстоятельство больше не составляет никакой проблемы.
«Мы убедились, что метод AlphaFold2, разработанный DeepMind, работает как в простых, так и в очень сложных случаях. Это настоящий прорыв! Теперь искусственный интеллект способен сделать то, чего не может сделать ни один человек даже с самыми глубокими познаниями в области моделирования белков», — говорит Торстен Шведе из Базельского Университета. Возможен этот прорыв стал благодаря тому, что искусственный интеллект AlphaFold2, разработанный DeepMind, использует самые передовые методы машинного самообучения на основе нейрональных сетей, что позволяет прогнозировать возможные структуры еще неведомых белков непосредственно на основе их генных секвенций (последовательностей).
С этой целью AlphaFold2 собрал, используя предоставленные научным сообществом итоговые данные экспериментов, информацию о последовательностях и структуре почти 100 тыс. известных белков и теперь он может создавать высокоточные прогнозные 3D-модели для практически любого мылимого протеина. Исключительность достижений DeepMind была подтверждена и сертифицирована организаторами эксперимента Critical Assessment of protein Structure Prediction (CASP). По их словам, «расчёты и предсказания, полученные AlphaFold2, являются «беспрецедентными».
Уточним, что эксперимент CASP («Критическая оценка степени точности прогнозирования структуры белка») проводится на международном уровне раз в два года для оценки прогресса в области соответствующих технологий. В ходе испытаний, проведённых в 2020 году (сессия CASP14Внешняя ссылка), точность методов прогнозирования была протестирована почти на ста видах протеинов. Прогнозы AlphaFold2 оказались очень точными даже в самых сложных случаях, таких, например, как вирусы SARS-CoV-2 и SARS-CoV-2 ORF8, каждый из которых состоит из примерно 30-ти различных видов белков, дюжина из которых пока все еще очень мало изучена.
Золотое правило прогресса
Успех компании DeepMind отчасти объясняется активной поддержкой со стороны научного сообщества и наличием открытого обмена информацией в области вычислительной структурной биологии, чему также способствовал успех проекта с сервером SWISS-MODEL. По словам Торстена Шведе, информацию, необходимую для решения этой одной из самых сложных проблем в биоинформатике, компания DeepMind получила только благодаря свободному обмену структурными данными и достижениями в области передовых методов вычислений.

Показать больше
Никлаус Вирт — живая легенда информатики из Швейцарии
Во время пандемии обмен такими данными дополнительно активизировался, и этот факт продемонстрировал, что международное сотрудничество жизненно необходимо для достижения быстрых результатов и решения таких актуальных задач, как создание вакцины от коронавируса. «Мы многому научились во время этой пандемии. Только открытый обмен информацией о вирусе SARS-CoV-2 в научном сообществе и позволил разработать вакцины в рекордные сроки», — добавляет Торстен Шведе, отмечая, что это доказывает, насколько контрпродуктивным для научных исследований может быть старое мышление, действующее по принципу «своя рубашка ближе к телу».

Показать больше
Совместим ли искусственный интеллект с европейскими ценностями?

В соответствии со стандартами JTI
Показать больше: Сертификат по нормам JTI для портала SWI swissinfo.ch



















Примите участие в дискуссии