Cautela en Suiza sobre la extracción de implantes
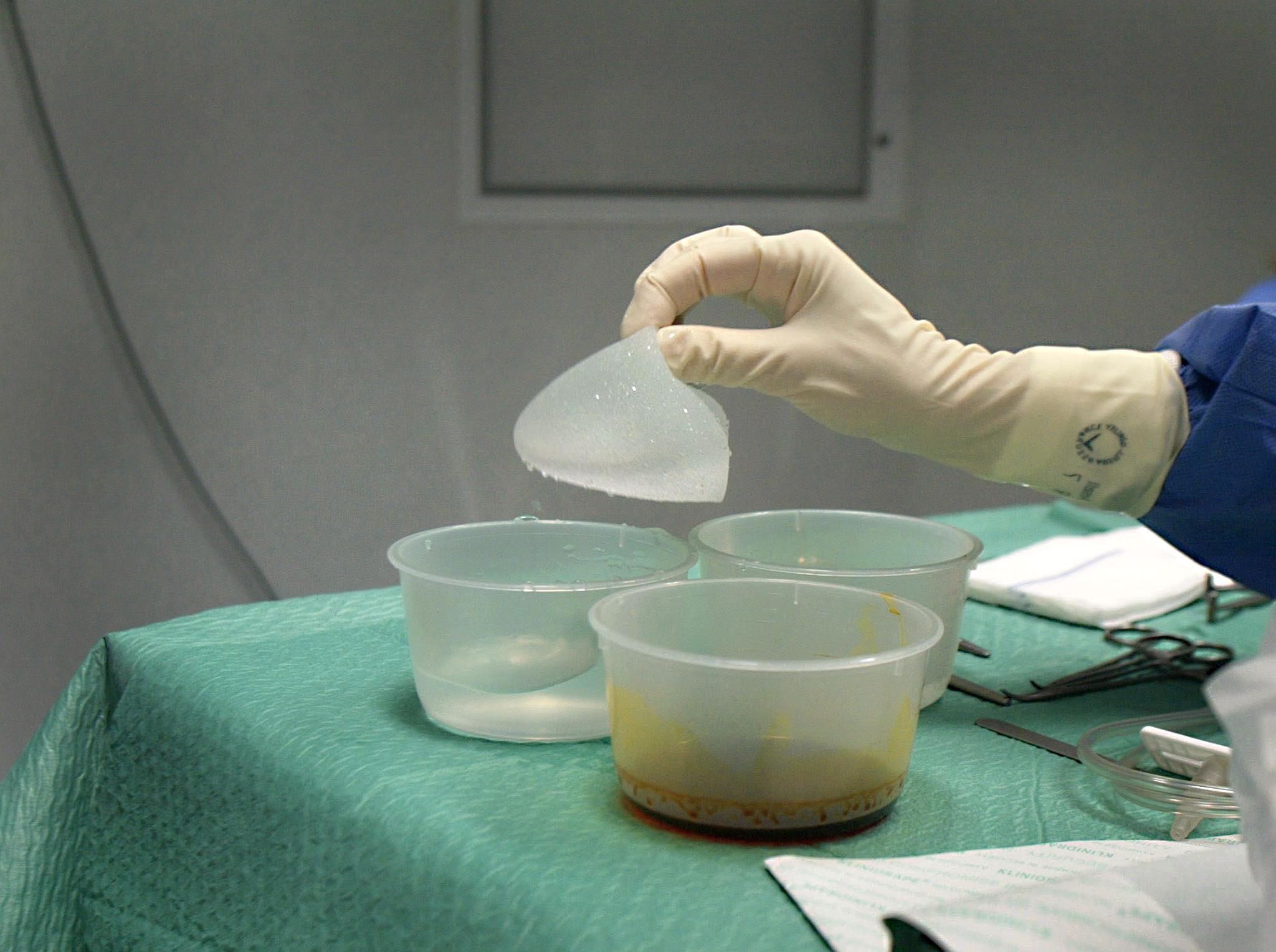
Las autoridades sanitarias helvéticas afrontan con cautela la alarma desatada por el caso de los implantes mamarios franceses, en diversos países del mundo. En Suiza, algunas mujeres ya están pasando a la acción.
El regulador suizo de control de medicamentos, ‘Swissmedic’, se aferra a su línea de que los implantes defectuosos realizados por la firma francesa Poly Implant Prothèse (PIP), ahora en bancarrota, por lo general no deben ser retirados.
Es una decisión contestada por los fundadores de una nueva asociación creada en Ginebra en los últimos días.
Victimes du 95c (nombre de una talla de sujetador) ha criticado la política suiza sobre el tema y ha presentado una solicitud ante la fiscalía de Ginebra para lanzar una investigación criminal sobre PIP por la venta de “los implantes mamarios fraudulentos” en Suiza.
Más de 400.000 mujeres en todo el mundo compraron los implantes PIP antes de que la compañía cerrara en 2010. Una inspección oficial reveló que PIP utilizó silicona industrial, no aprobada, en algunos de sus productos.
Las pruebas mostraron que las coberturas del implante presentan un mayor riesgo de ruptura -un factor que llevó a Francia a recomendar a 30.000 mujeres con estos implantes que se los retiraran como medida preventiva. La República Checa, Alemania y los Países Bajos están dando el mismo consejo.
El número de mujeres afectadas en Suiza es minúsculo en comparación. Se estima que alrededor de 280 mujeres portan este tipo de implantes.
Sin embargo, para el grupo Victimes du 95c, el riesgo sigue siendo importante. De acuerdo con un archivo enviado al fiscal de Ginebra, la asociación asegura que la vida de estas mujeres está en peligro, debido al uso de la silicona barata y la baja calidad de sus implantes.
Suiza no está haciendo lo suficiente, afirmó la asociación. “Es como si este problema de salud, que preocupa al resto de Europa, se hubiera detenido en la frontera”. Así, pidieron al fiscal de Ginebra que prohíba en el futuro el uso de los implantes mamarios controvertidos.
Enfado
La política ginebrina, Salika Wenger, creó el grupo. “Cuando vimos la respuesta de Swissmedic -de que esta (cuestión) no era muy grave y que apenas afectó a nadie- las mujeres que tenían problemas reales se enfadaron mucho”.
Wenger dijo que sabía de un caso en el que los implantes se habían roto y se filtraron en el cuerpo de la portadora.
“No hay muchas entre nosotras, solo una docena. Pero desde el lanzamiento, muchas personas me han llamado o enviado correos electrónicos para decirme que también tenían problemas y que querían ser parte de la asociación”, relata a swissinfo.ch.
“Creemos que ‘Swissmedic’, que tiene la tarea de ver si los productos se deben introducir en el mercado o no, no ha hecho su trabajo. Creemos que las autoridades públicas, especialmente en el gobierno, no están tomando en serio su trabajo”.
De hecho, ‘Swissmedic’ es responsable principalmente del control de los medicamentos que salen al mercado. El control de calidad de los dispositivos médicos, como los implantes de mama, se inscribe en el marco de las relaciones bilaterales del país con Europa, y como tal, sigue los procedimientos europeos.
En el caso de los implantes PIP, en Europa fueron autorizados por un organismo regulador de Alemania; recibieron la “marca CE”, una calificación que indica que cumple con las leyes de sanidad y seguridad de la Comisión Europea.
Una vez que un producto lleva la marca CE se puede distribuir en Europa sin la necesidad de pasar más controles. Es un sistema informal que ha sido criticado por los médicos en el pasado.
“’Swissmedic’ no vuelve a controlar estos productos. Una vez que el cuerpo de notificación dice que está bien, como médico usted puede comprar este producto y utilizarlo”, explica a swissinfo.ch el portavoz de Swissmedic, Daniel Lüthi.
‘Swissmedic’ interviene cuando los productos son defectuosos. Por ejemplo, mediante la información a los pacientes sobre el problema con los implantes PIP.
“Los hospitales que utilizan el producto tienen que comprobar si hay malas experiencias, fugas o incidentes e informarnos si hubiera este tipo de casos. Así intercambiamos esta información con otras autoridades”, según Lüthi.
Cambiar el status quo
Bajo el sistema actual, mucha de la responsabilidad de dichos implantes recae en los médicos, que deberían saber “lo que se implanta”, indica Lüthi.
El status quo europeo podría cambiar, sin embargo, a la luz del escándalo de los implantes mamarios. A principios de este mes, el nuevo jefe del Observatorio Europeo sobre Drogas planteó la necesidad de fortalecer las regulaciones sobre los productos sanitarios.
“No veo una necesidad urgente de adoptar para el material médico las mismas medidas de seguridad que para los medicamentos”, declaró Guido Rasi, director ejecutivo de la Agencia Europea de Medicamentos (EMA), a Reuters.
El miedo a los implantes mamarios, dijo, puede acelerar los cambios de las normas que rigen el sector de la tecnología médica. En opinión de ‘Swissmedic’, “si Europa, por ejemplo, decide cambiar algo en estas recomendaciones, por supuesto no tendremos ninguna razón para no hacerlo porque somos parte de esta red internacional”, añade Lüthi.
Mientras tanto, la agencia discute el tema con otros países e intercambia los datos más recientes. Por el momento, no ve ninguna razón para cambiar sus directrices.
Los implantes mamarios de silicona fueron fabricados por la empresa Poly Implant Prothèse (PIP), creada en 1991 en el sur de Francia.
Esta compañía fue considerada la tercera en el mundo en volumen de ventas de prótesis, al producir unas 100.000 al año.
De éstas, el 80% se exportaba.
El problema principal de las PIP es que su índice de rotura es mucho mayor que el de otras prótesis mamarias (que es de un 0,5%-1%), aunque ese porcentaje varía según la fuente consultada y oscila entre un 7% y un 12% en tres años.
Aunque el uso de estas prótesis se suspendió en Francia y España en 2010 debido a la alta tasa de roturas, la nueva alarma saltó a mediados del pasado mes de diciembre tras la aparición de ocho casos de cáncer entre las portadoras de las prótesis.
Se estima que, en todo el mundo, entre 400.000 y 500.000 mujeres podrían llevar prótesis de este tipo, aunque no se conoce el número exacto ya que la empresa podría haber comercializado estas prótesis con otro nombre, tal y como ocurrió en Holanda.
(Adaptación: Iván Turmo Ferrer)

En cumplimiento de los estándares JTI
Mostrar más: SWI swissinfo.ch, certificado por la JTI




Puede encontrar todos nuestros debates aquí y participar en las discusiones.
Si quiere iniciar una conversación sobre un tema planteado en este artículo o quiere informar de errores factuales, envíenos un correo electrónico a spanish@swissinfo.ch.