
史上最貴的天價藥怎麼了?

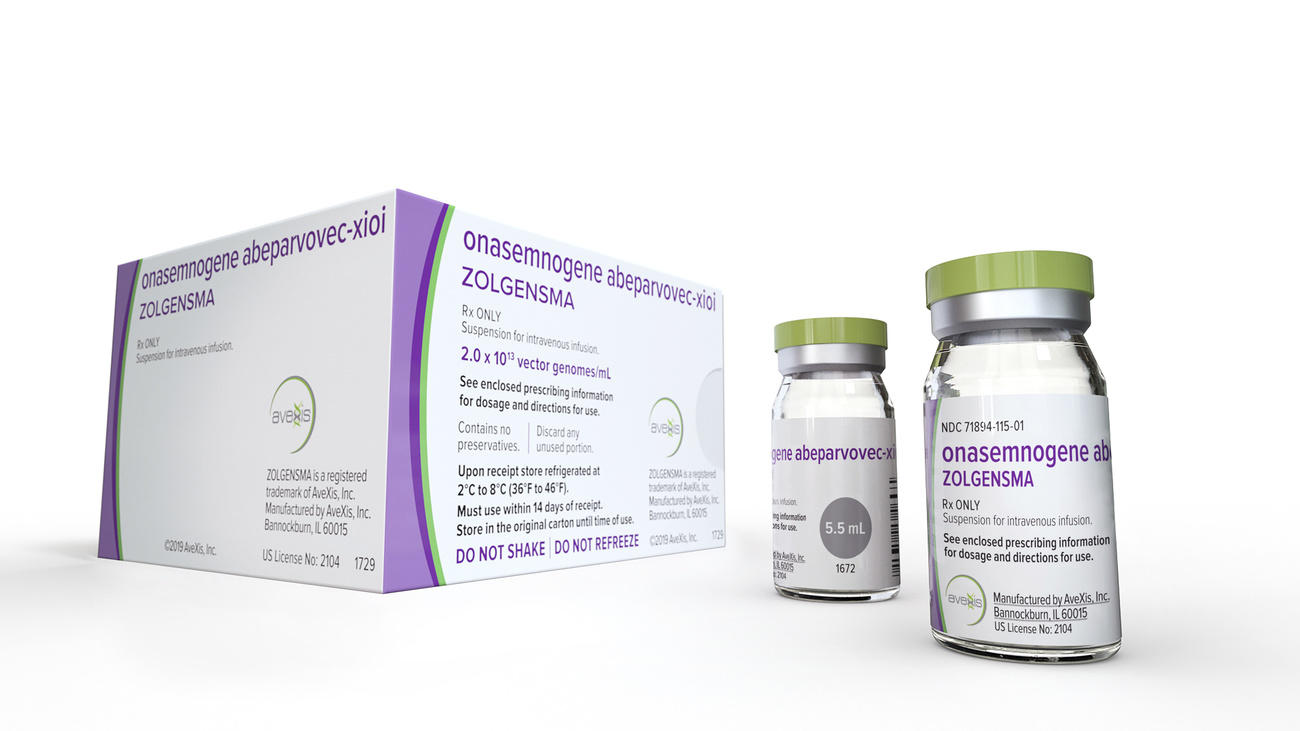
Zolgensma是單次性治療藥物,用於治療患有罕見致命遺傳疾病的嬰兒,五年前以210萬美元的天價投放市場。但由於年銷售額開始下降,新市場又難以開拓,該藥的瑞士生產商諾華公司(Novartis)面臨越來越大的壓力。
阅读本文简体字版本请 点击这里
訂閱我們的時事通訊電子報(Newsletter),每週您會在您註冊的信箱中收到一封免費電子郵件,內容是瑞士資訊繁體中文版報導。請擊點這裡,現在就訂閱。
今年1月,諾華執行長萬思瀚(Vas Narasimhan)在公佈公司2023年度業績時,甚至隻字未提Zolgensma。2019年這款藥物上市時備受矚目,它是首個治療脊髓性肌肉萎縮症(SMA)的基因藥物,脊髓性肌肉萎縮症是一種罕見的神經肌肉疾病,也是全球嬰兒死亡的重要遺傳因素 。
這種單次性注射藥物最初被宣傳為脊髓性肌肉萎縮症的潛在治癒方案,有望成為這家瑞士製藥巨頭六大成長引擎之一,具有數十億美元的銷售潛力。當時分析師的一致預期是,這款藥物年銷售額可達19億美元,但一家投資銀行預測的年銷售額卻高達28億美元。在歐洲藥品管理局於2020年核准此藥物附條件上市後,其2021年銷售額年增46%,達13.5億美元。
但阿哌奧諾基(商品名為Zolgensma)未能保持強勁的銷售動能。以美元計算,2022年的全球銷售額僅成長了1%,2023年則下降了11%,降至12.1億美元。 在其最大的單一市場美國,去年銷售額下降了14%至3.72億美元,這是連續第二年下降。
羅蘭貝格顧問公司蘇黎世辦公室執行合夥人馬蒂亞斯‧邦特(Matthias Bünte)對此並不感到意外,他專注於研究製藥公司的市場拓展和成長策略。邦特說:「這款藥物在主要市場度過最初的成長階段後,銷售額會受到符合用藥條件的脊髓性肌肉萎縮症患者出生率的限制。」對於單次性治療藥物而言,這是意料之 中的情況。它與慢性病藥物不同,後者可以透過不斷增加的新患者持續創造收入。
Zolgensma銷售額下降並逐漸淡出諾華財報電話會議,與公司在2018年收購該藥物研發機構AveXis時的樂觀預期形成了鮮明對比。諾華當時以87億美元收購這家納斯達克上市的新創公司,意在增強其基因療法業務。
諾華公司的發言人在聲明中向瑞士資訊swissinfo.ch表示:「銷售額成長趨緩的一個重要原因是,[美國等]成熟市場現在主要治療的是新發病例而非現有病例。」
諾華公司發現,要打入美國和歐洲相對富裕國家以外的市場頗具挑戰,因為醫療預算吃緊的各國政府質疑這種藥物的療效是否足以證明其價格的合理性。
相关内容
“史上最贵药”,何以卖出1465万元人民币的天价?
美國食品藥物管理局(FDA)被廣泛認為是全球藥物核准的黃金標準。2019年,FDA率先批准Zolgensma上市,當時諾華公司為其定價210萬美元,使其成為有史以來最昂貴的單次性治療藥物。
儘管截至2024年1月,Zolgensma已在51個國家獲批上市,並治療了3’700多名患者,但只有35個國家提供商業報銷,這使得許多脊髓性肌肉萎縮症患者無力負擔這種救命藥,有些人只能透過群眾募資來籌集治療費。
證明價格的合理性
全球大約每1萬名嬰兒中就有1人患有脊髓性肌肉萎縮症,在美國每年約有300名嬰兒患病。 它是由SMN1基因突變引起,這種基因突變導致細胞無法產生足夠的SMN蛋白,而這種蛋白負責向肌肉發送重要訊號。 這種蛋白不足會損害運動神經元,導致肌肉弱化。
如果不進行治療,患有最嚴重脊髓性肌肉萎縮症的嬰兒可能永遠無法抬頭或抬腿,吞嚥和呼吸也會很困難。這些嬰兒大多在兩歲前因呼吸問題而死亡。成人也可能患有脊髓性肌肉萎縮症,但往往症狀較輕。
治療脊髓性肌肉萎縮症等罕見疾病的藥物通常需要數年時間和數十億美元才能研發出來。藥企將這些藥物的價格定得很高,以收回投資並彌補銷售量的不足。
諾華公司為Zolgensma的定價辯稱,這是一種單次性注射藥物,針對疾病的基因根源問題。透過將正常的基因替換有缺陷的基因,這種藥物不僅能挽救生命,還能免於家庭和公共衛生系統昂貴的終身治療費用。
在基因療法上市之前,唯一可用於治療脊髓性肌肉萎縮症的藥物是美國渤健公司(Biogen)於2016年推出的諾西那生鈉注射液(商品名為Spinraza),患者需接受終生治療,每年藥費在30萬至50萬美元。如果接受十年的治療,這種每年進行三次脊髓注射的藥物總費用將遠遠超出Zolgensma 210萬美元的售價。
諾華公司並未解釋Zolgensma的具體定價方式,而獨立評估機構對其公允定價的計算差異巨大–從71萬美元到210多萬美元不等–這也導致諾華這款天價藥物的定價理由面臨更多爭議 。
當這種藥物高價上市時,實際接受治療的患者數量極少,這也引發了人們對其真正價值的質疑。與許多治療危及生命的罕見疾病的藥物一樣,Zolgensma在美國、歐洲和日本透過加速審批上市,讓患者更快使用這種救命藥。
美國食品藥物管理局的批准決定是基於已完成的早期試驗和正在進行的晚期試驗,這兩項試驗共涉及不到40名患者。大多數注射Zolgensma的嬰兒都存活了下來,能夠自主呼吸,並在用藥兩年後達到了一些重要里程碑,例如自主坐立。
然而,治療效果有顯著差異,部分兒童出現了嚴重的副反應,包括肝臟損傷。 此外,由於試驗時間較短,關於藥物療效持續時間的數據尚缺乏。美國以外的試驗參與者也很少。
在美國及一些富裕國家,Zolgensma被限定用於患有最嚴重脊髓性肌肉萎縮症的最年幼患者(兩歲以下),因為在這些國家,Zolgensma的安全性和有效性證據最為充分。
歐洲藥品管理局核准該藥物用於體重不超過21公斤的兒童,包括5歲及以下的幼兒,但許多歐盟成員國祇報銷6個月以下兒童的治療費用。
高藥價阻礙治療
由於在成熟市場的成長潛力有限,拓展Zolgensma的地域覆蓋範圍對諾華來說至關重要。但是,考慮到其他醫療需求也要投入資源且整體預算有限,許多中等收入國家希望看到更多證據,證明這種藥物的定價具備合理性。
薇拉·佩佩(Vera Pepe)向瑞士資訊表示:「對於罕見疾病,我們面臨的挑戰是,我們需要快速獲得藥物,但同時藥物價格又非常高,而且存在很多不確定因素。有時我們無法確切知道藥物真正的臨床療效中。」
經過兩年多的價格和條款談判後,巴西政府與諾華公司最終在2022年底達成協議。諾華同意以110萬美元的單次注射價格為不超過250名嬰兒提供治療,並承諾在巴西進行該藥物治療的長期效果研究。
但包括土耳其在內的其他國家仍以安全性和有效性證據不足為由拒絕使用這種藥物。
全球藥品定價和退款管理解決方案提供商Lyfegen的執行長吉里沙·費爾南多(Girisha Fernando)表示:「藥廠不能再僅僅向市場推出售價200萬美元的藥品,並指望政府為其買單。他們需要提供的不僅僅是這些。」
諾華表示希望能讓中等收入國家也能用上Zolgensma,並正在向保險機構和國家衛生部門提供折扣、分期付款計劃和風險分擔協議,使其根據事先商定的治療效果進行支付。
去年,諾華與阿根廷國家醫療支付機構簽訂了這樣一份協議,以130萬美元的單價提供Zolgensma。根據Lyfegen協議庫中的一份合約副本,只有「根據現有科學證據,在患者身上觀察到的結果符合預期」時,才會進行支付。
對於脊髓性肌肉萎縮症兒童的家庭來說,等待藥物治療的過程非常煎熬。患病孩童延遲治療的時間越長,病情就會惡化得越厲害,而Zolgensma也無法逆轉病情的進展。
數據困境
諾華公司在某種程度上得益於更多的臨床試驗結果,以及來自全球醫療服務提供者的所謂「真實世界數據」。 這些數據顯示,許多接受該療法的患者都取得了積極的療效。
2023年3月,諾華自行進行的研究表明,嬰兒時期注射Zolgensma的患者在用藥7年後仍能保持主要的運動里程碑,例如坐立,並能在無輔助的情況下呼吸。病情較輕的大齡兒童在註射較高劑量的新版Zolgensma後,病情也有所改善。
相关内容
瑞士初创公司颠覆全球医药付费模式
不過,部分患者的病情並沒有進一步改善,81名參與研究的兒童中有24名後續轉而使用其他脊髓性肌肉萎縮症藥物。其他研究,包括瑞士一項涉及九名患者的研究,也突顯出潛在結果的巨大差異。
越來越多的試驗和治療結果表明,最初關於Zolgensma能夠一次治癒脊髓性肌肉萎縮症患者的炒作並沒有在現實世界中得到證實。
家長們期盼自己的孩子能被治癒,因為這種基因療法上市之初就是這樣被宣傳的。歐洲脊髓性肌肉萎縮症患者權益組織和瑞士脊髓性肌肉萎縮症患者權益組織的負責人妮可·古塞特(Nicole Gusset)告訴瑞士資訊:「這讓人們對一種非常複雜且仍未被完全理解的疾病產生了不合理的治療預期。」女兒也患有脊髓性肌肉萎縮症。
隨著其他治療脊髓性肌肉萎縮症的藥物陸續上市,諾華面臨的壓力也增加。 2020年,美國食品藥物管理局批准瑞士羅氏公司(Roche)的利司撲蘭(商品名為Evrysdi)上市銷售,用於治療年齡較大的兒童患者以及成人患者。近期,這款藥物的適用人群經批准擴大到兩個月以下的嬰兒,這使其成為Zolgensma更直接的競爭。
Evrysdi有藥丸和糖漿兩種口服劑型,比基因療法更容易給藥,年費用在10萬至35萬美元之間,取決於患者的體重。Evrysdi已在100多個國家獲準上市,並已治療全球11’,000多位脊髓性肌肉萎縮症患者。
古塞特說:「所有這些藥物都能控制疾病的進展。現階段我們還不清楚哪種藥物對哪些人群或哪些個體最有效。」
合理定價
其他投入數十億美元研發新藥的基因療法研發機構正密切關注這家瑞士製藥巨頭如何應對這些不利因素。目前在美國有超過1’500項有關細胞和基因治療的註冊臨床試驗,去年美國食品和藥物管理局共批准了五款相關新藥上市,其中包括兩種治療鐮狀細胞病的藥物,它們的定價 比Zolgensma還高,分別為220萬美元和310萬美元。
今年3月,Orchard Therapeutics公司的基因治療藥物Lenmeldy(又稱Libmeldy)在美國創下了425萬美元的藥價紀錄,這款藥物用於治療異染性腦白質營養不良,這是一種侵襲幼兒中樞 神經系統的極罕見遺傳疾病。在美國,這種疾病每年影響約40名新生兒。
藥品定價專家、蘇黎世大學法律與醫學系教授科爾斯汀·諾埃勒·沃金格(Kerstin Noëlle Vokinger)指出:「政府面臨著向患者提供新藥的壓力。這可以理解,因為罕見或致命疾病 患者需要治療。」
編輯:Nerys Avery,編自英文:瑞士資訊中文部/dh,繁體校對:方常均

符合JTI标准






















您可以在这里找到读者与我们记者团队正在讨论交流的话题。
请加入我们!如果您想就本文涉及的话题展开新的讨论,或者想向我们反映您发现的事实错误,请发邮件给我们:chinese@swissinfo.ch。