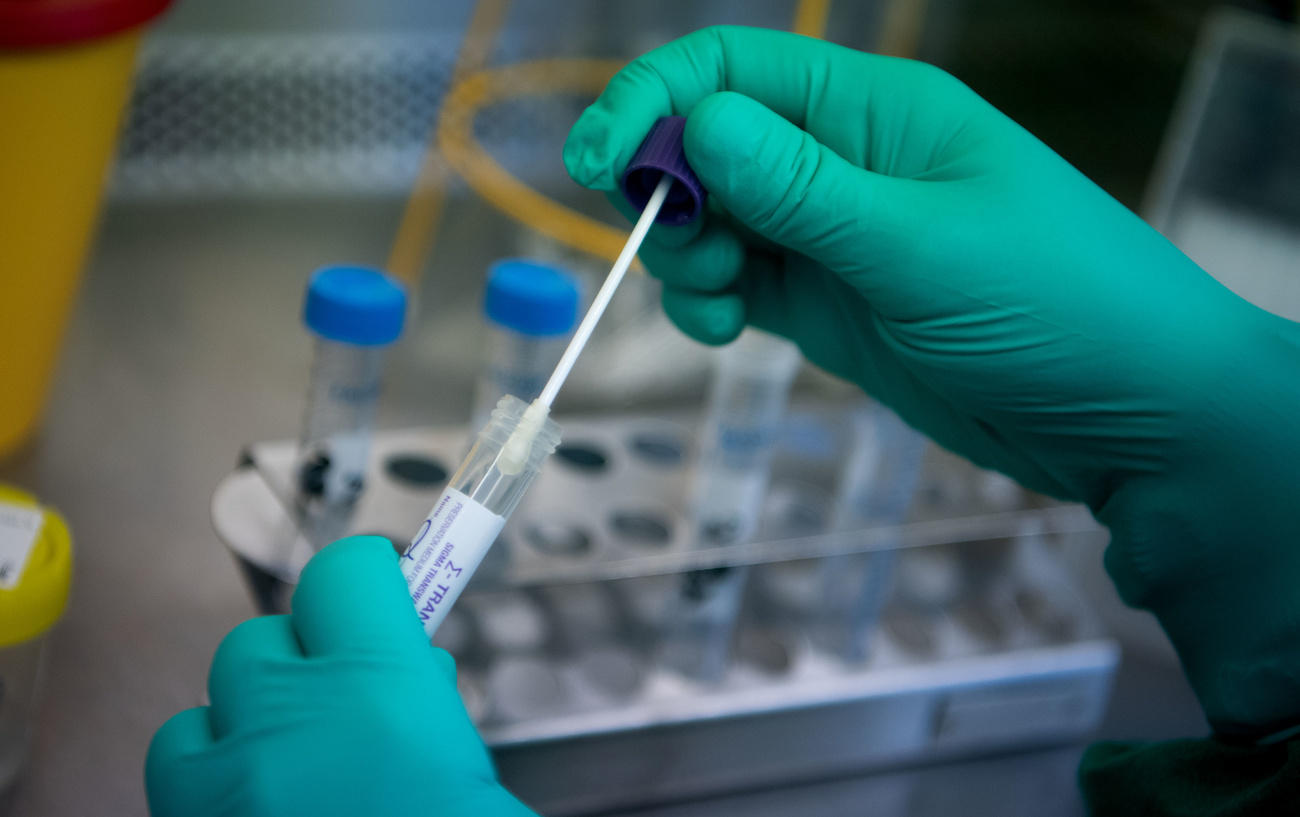
 由罗氏开发的这项新冠病毒抗体血清学检测技术,可通过受测试者血样,检测出其是否已产生应对新冠病毒的抗体。
Copyright 2020 The Associated Press. All Rights Reserved.
由罗氏开发的这项新冠病毒抗体血清学检测技术,可通过受测试者血样,检测出其是否已产生应对新冠病毒的抗体。
Copyright 2020 The Associated Press. All Rights Reserved.
瑞士制药巨擘罗氏制药(Roche)于5月3日宣布,由该公司开发的Elecsys Anti-SARS-CoV-2新冠病毒抗体血清学检测技术,现已获美国食品药品管理局(FDA)紧急使用授权。
此内容发布于
罗氏旗下的这项新冠病毒抗体检测技术,是为了判断受检测者此前是否接触并感染过新冠病毒、以及是否已经产生了应对2019冠状病毒病的抗体而设计的。
据总部位于瑞士巴塞尔的罗氏制药介绍,其开发的Elecsys Anti-SARS-CoV-2新冠病毒抗体检测技术,特异度(编者注:又称为“真阴性率”,特指实际阴性样本中被判断为阴性的比例,计算方法为真阴性除以真阴性+假阳性)高达99.8%,从而有效降低了产生假阳性检测结果的可能性;与此同时,这项技术在检测抗体方面的灵敏度达到了100%。
罗氏已开始向遍布全球各地的实验室运送这款全新的抗体检测试剂盒,并表示计划将试剂盒产量在现有产能基础上提升到“每月数千万套”,从而保障面向美国和接受CE安全认证的诸多国家的供应。
由于抗体检测结果能够帮助各国决策者加深对2019冠状病毒病的了解、判断哪些人有可能已经感染上了新冠病毒、而哪些人或许已经具有了免疫力、从而确定还需要采取哪些措施来对抗疫情,因此目前,世界各地的研究人员都在竞相开发血清学检测(即抗体检测)。
相关内容

相关内容
新冠疫情:瑞士局势
此内容发布于
这里,瑞士资讯swissinfo.ch为您实时更新报道瑞士疫情发展:追踪最新病毒感染数据、公告瑞士联邦防疫措施、介绍官方健康防护信息和重要咨询途径。
更多阅览 新冠疫情:瑞士局势

相关内容
苏黎世州不希望为未成年人实施性别重置手术
此内容发布于
瑞士在性少数群体权益保护方面称不上先锋,直至2022年同性婚姻合法化,才算与许多其他西欧国家接轨。随着人们对性别重置手术的态度越发谨慎,苏黎世州率先提出该领域需要更加规范。
更多阅览 苏黎世州不希望为未成年人实施性别重置手术

相关内容
瑞士对移民的看法已经“过时”
此内容发布于
瑞士因其政治人文和自然环境优势,以及高额的薪资成为高度国际化的国家。前往瑞士的移民一度以寻求庇护的难民为主,如今,大量的高素质移民为推动其经济增长做出了巨大贡献。
更多阅览 瑞士对移民的看法已经“过时”

相关内容
建筑密度不一定会导致城市升温
此内容发布于
拥挤的空间自带热感,这也是为什么大家都会觉得城市密度化导致升温。作为在有限土地上拓展居住空间的手段,密度化似乎不可避免。不过,瑞士专家表示,密度不是问题,如何布局才是关键。
更多阅览 建筑密度不一定会导致城市升温

相关内容
吉娃娃营救冰川裂缝中的主人
此内容发布于
7月4日,一只吉娃娃协助救出了它在费冰川(Fee Glacier)上被困的主人。它向救援队发出信号,指引救援人员找到掉入冰川裂缝中的男子。
更多阅览 吉娃娃营救冰川裂缝中的主人

相关内容
ABB拓展在华机器人业务
此内容发布于
4月,ABB集团表示拟分拆机器人业务独立上市,并计划在2026年第二季度完成100%分拆。与此同时,ABB于近日宣布拓展在华业务,引进三款新型机器人系列,用于电子、消费品工业、制造业等高速发展的领域。
更多阅览 ABB拓展在华机器人业务

相关内容
中国电商平台Temu欲进军瑞士食品市场
此内容发布于
媒体报道称,中国电商平台Temu正在为进入瑞士食品零售市场做准备。瑞士德语日报《每日导报》透露,继德国市场启动后,Temu开始对瑞士市场跃跃欲试。
更多阅览 中国电商平台Temu欲进军瑞士食品市场

相关内容
跟踪行为在瑞士将被视作刑事犯罪
此内容发布于
Swiss parliament has voted in favour of making stalking a criminal offence.
更多阅览 跟踪行为在瑞士将被视作刑事犯罪

相关内容
欧盟公民前往瑞士主要目的是工作
此内容发布于
经济的发展离不开强有力的劳动力市场。瑞士联邦统计局的预测显示,瑞士人口增长自2035年起将完全依靠移民。联邦经济事务秘书处近日的报告也指出,瑞士的劳动力市场大门必须保持敞开。
更多阅览 欧盟公民前往瑞士主要目的是工作

相关内容
欧洲最快乐的退休老人住在瑞士
此内容发布于
如果预算充足,想在欧洲养老,选哪个国家呢?瑞士人寿保险公司的一份调查为你贴心指路。欧洲最快乐的老年人住在瑞士。他们不仅身体健康,对自己的社交娱乐生活也相当满意。
更多阅览 欧洲最快乐的退休老人住在瑞士

相关内容
世界上每六个人中就有一个生活在孤独中
此内容发布于
在数字时代,我们可以通过视频与异国他乡的亲人实时交流。但你知道吗?恰恰是这样的便利阻断了人们面对面的沟通渠道。全世界每六个人中就有一个人生活在孤独中。
更多阅览 世界上每六个人中就有一个生活在孤独中
阅读更多

相关内容
部分瑞士医院将推行新冠病毒免疫检测
此内容发布于
目前,数家瑞士医院正筹备展开血液检测,从而评估瑞士当前已有多少人感染了新冠病毒-其中也包括那些可能已经对新冠病毒具备免疫力的人。
更多阅览 部分瑞士医院将推行新冠病毒免疫检测

相关内容
日内瓦逾5%未被发现感染病例,远未达到群体免疫所需最低感染比例
此内容发布于
瑞士日内瓦州所进行的一项血清抗体检测初步评估结果显示,估测日内瓦州已有超过5%的常住居民,即2.7万人可能已感染了新冠病毒。该州感染规模虽超过官方统计的确诊病例数据,然而却低于研究人员此前期望实现“群体免疫”的人口感染预估比例。
更多阅览 日内瓦逾5%未被发现感染病例,远未达到群体免疫所需最低感染比例
相关内容
罗氏“昼夜不停”提供新冠病毒检测
此内容发布于
瑞士制药巨擘罗氏(Roche)表示,继其研发的高度自动化新冠病毒检测系统获批之后,目前,该公司正夜以继日、昼夜不停地全天候赶工,以期提供尽可能多的检测。
更多阅览 罗氏“昼夜不停”提供新冠病毒检测






































您可以在这里找到读者与我们记者团队正在讨论交流的话题。
请加入我们!如果您想就本文涉及的话题展开新的讨论,或者想向我们反映您发现的事实错误,请发邮件给我们:chinese@swissinfo.ch。