
La nuova legislazione farmaceutica europea è accolta con scetticismo in Svizzera

La Svizzera segue da vicino l'importante revisione delle norme che regolamentano i prodotti farmaceutici in Europa. Se da un lato l'industria chiede maggiori incentivi all'innovazione, dall'altro gli Stati membri vogliono dei medicamenti a prezzi più accessibili.
La Commissione europea ha pubblicato il 26 aprile la bozza tanto attesa della revisioneCollegamento esterno della legislazione sui prodotti farmaceutici. Si tratta di un tentativo per contenere i prezzi dei farmaci, migliorare l’accesso ai medicamenti innovativi quali le terapie geniche ed evitare le penurie di prodotti farmaceutici che si sono aggravate negli ultimi anni.
Le modifiche proposte sono di ampio raggio e vanno dalla riduzione dei tempi di approvazione dei nuovi farmaci al miglioramento della trasparenza dei finanziamenti pubblici per lo sviluppo dei medicamenti, fino all’accelerazione della distribuzione dei farmaci in caso di emergenza.
Altri sviluppi
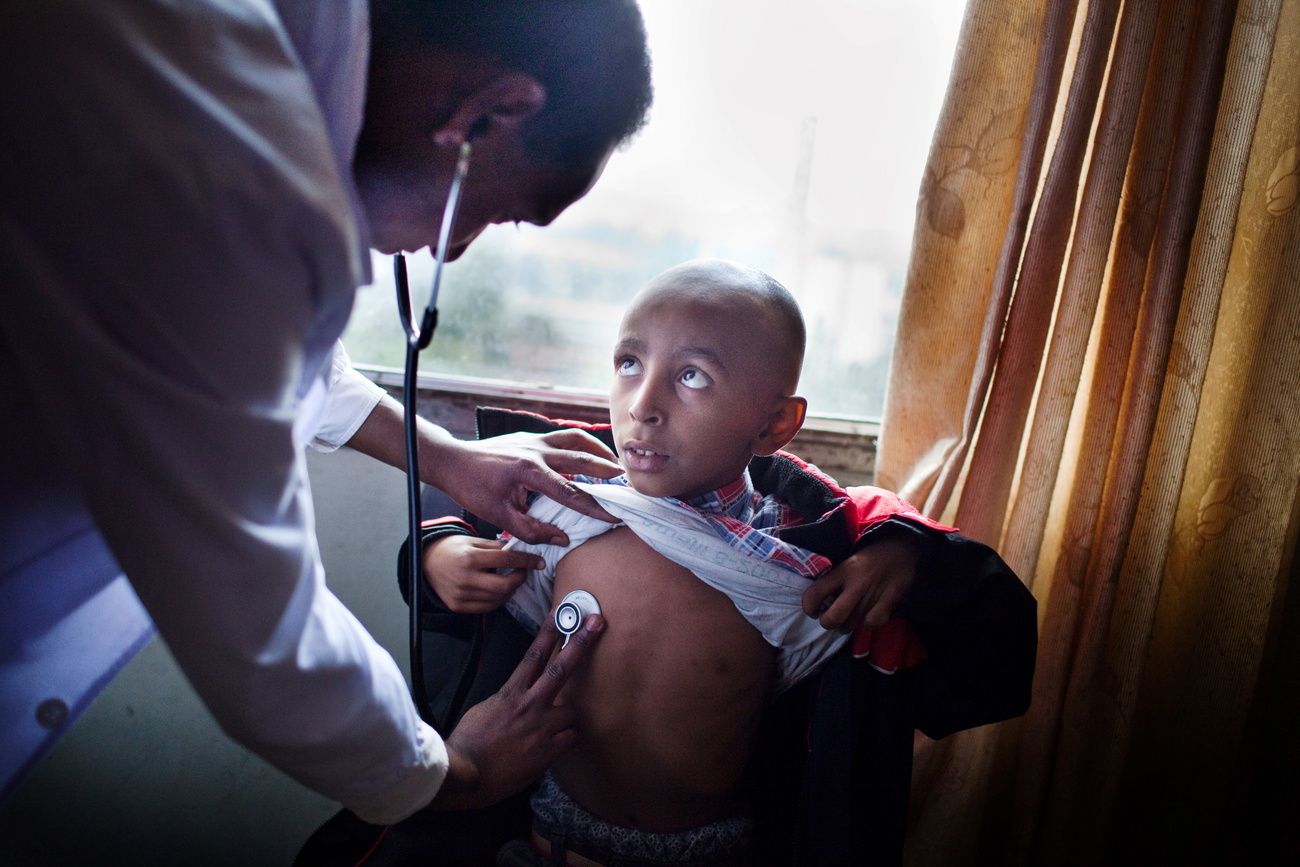
La fine dei farmaci a prezzi accessibili
Le reazioni nell’Unione Europea sono state contrastanti. L’industria farmaceutica sostiene che la nuova regolamentazione rischia di ostacolare l’innovazione nell’UE. Una parte di chi difende il sistema di salute pubblicaCollegamento esterno afferma invece che la revisione rappresenta un progresso, ma che alcune disposizioni chiave sono state rese meno incisive dalle lobby farmaceutiche.
Anche in Svizzera, che non fa parte dell’UE, la bozza è stata accolta con cauto ottimismo. ONG, politici e gruppi industriali hanno dichiarato di accogliere con favore la riforma, di cui c’era urgentemente bisogno, ma ci sono opinioni diverse sulla sua efficacia nell’affrontare i problemi.
“L’intenzione di rafforzare la competitività del continente e di preparare il futuro del quadro normativo europeo è stata ben accolta dall’industria”, ha scritto René Buholzer, direttore dell’associazione delle imprese farmaceutiche svizzere Interpharma, in un articolo di opinioneCollegamento esterno pubblicato sul quotidiano francofono Le Temps. “Tuttavia, le proposte che ne derivano rischiano di complicare il quadro normativo e di indebolire gli incentivi a investire nell’innovazione”.
Il progetto di legge, la prima revisione da circa 20 anni, giunge in un momento di accesi dibattiti su come incoraggiare l’innovazione senza che i prezzi elevati possano spingere i sistemi sanitari ai loro limiti.
Il linguaggio utilizzato riflette il delicato equilibrio che sta cercando di raggiungere la leadership europea per tenere sotto controllo l’industria farmaceutica, senza per questo allontanarla dal proprio territorio. Diversi leader del settore hanno alimentato questi timori, sostenendo che l’Europa rischia di rimanere indietroCollegamento esterno rispetto al resto del mondo in materia di innovazione se la regolamentazione è troppo severa.
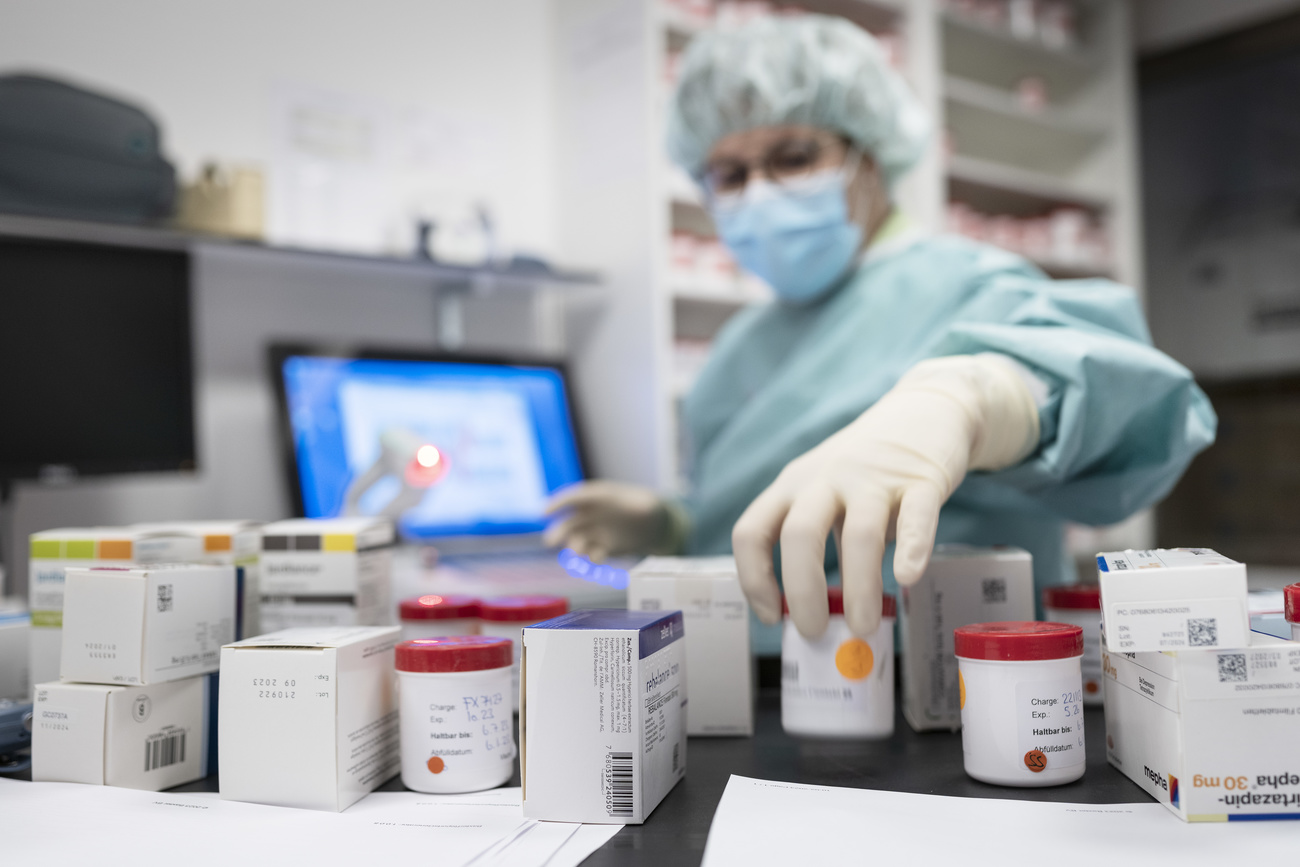
Altri sviluppi
Nel Paese dei farmaci stanno finendo le medicine
In febbraio, il CEO di Novartis, Vas Narasimhan ha dichiarato che le misure di riduzione dei costi in Europa erano molto preoccupanti e che stavano erodendo l’attrattiva dell’ecosistema dell’innovazione.
In un messaggio inviato via e-mail dopo la pubblicazione del disegno di legge, un portavoce di Roche ha dichiarato che l’azienda spera che “la nuova legislazione dell’UE per i prodotti farmaceutici garantisca che l’Europa rimanga una destinazione privilegiata per gli investimenti nelle scienze della vita, in un contesto di concorrenza in rapido aumento in tutto il mondo”.
Dare e avere
Questa ricerca di un equilibrio risulta evidente nel linguaggio relativo al periodo di esclusività, che conferisce a un’azienda il monopolio sulla vendita di un farmaco. Se le nuove norme saranno approvate, le aziende avranno a disposizione solo otto anni (una combinazione di protezione dei dati e protezione del mercato) invece di dieci anni di esclusività. Ciò è vantaggioso per i e le pazienti e per chi paga, come le compagnie assicurative, dato che le versioni più economiche di un farmaco arriverebbero prima sul mercato. L’industria, tuttavia, si oppone con veemenza ai cambiamenti che consentono alla concorrenza di intaccare i profitti.
La legislazione dell’UE stabilisce però che se un prodotto è commercializzato in tutti i Paesi membri e soddisfa varie condizioni, l’esclusività può anche essere superiore ai dieci anni. Si tratta di un compromesso, afferma Patrick Durisch, responsabile delle politiche di salute pubblica presso l’ONG Public Eye. “L’UE avrebbe potuto essere molto più severa adottando delle misure per migliorare l’accesso e riequilibrando i profitti ottenuti dalle aziende grazie ai loro monopoli”.
L’industria rimane comunque scettica. In una dichiarazione rilasciata dopo la presentazione della revisione legislativa, Nathalie Moll, direttrice generale della Federazione europea delle industrie e delle associazioni farmaceutiche, afferma che “penalizzare l’innovazione se un farmaco non è disponibile in tutti gli Stati membri entro due anni è fondamentalmente sbagliato e rappresenta un obiettivo impossibile per le aziende”.
La Svizzera pensa alla sua competitività
Il mondo politico e l’industria in Svizzera seguono con attenzione lo sviluppo del nuovo quadro normativo. L’UE non è solo un mercato importante per le aziende elvetiche, ma anche una fonte di personale. Roche ha circa 44’000 dipendenti in Europa (circa un quinto del totale) e investe nel continente all’incirca 6 miliardi di franchi svizzeri, pari al 40% della sua spesa globale per la ricerca e lo sviluppo.
La Svizzera sta però cercando di trovare un proprio equilibrio. Il Governo elvetico non vuole rifiutare nuove regolamentazioni e incrinare così le relazioni con l’UE, peraltro già traballanti dopo che nel 2021 la Svizzera aveva interrotto i negoziati per un accordo istituzionale con Bruxelles.

Altri sviluppi
Svizzera-UE: perché le relazioni sono così complicate?
Per la Svizzera, una delle priorità fondamentali nei colloqui in corso è l’accesso a Orizzonte Europa, il più grande programma di ricerca del l’UE con un bilancio di 90 miliardi di euro (88,3 miliardi di franchi).
La Svizzera dipende dall’UE anche in diversi settori, tra cui i protocolli comuni per la sicurezza dei e delle pazienti e il coordinamento nella gestione delle carenze di farmaci. Le aziende farmaceutiche elvetiche desiderano inoltre mantenere un accesso illimitato al mercato europeo.
Allo stesso tempo, la Confederazione tiene conto della sua competitività. La Svizzera concede l’esclusività dei farmaci per 20 anni, il che contribuisce ad attirare aziende innovative. L’adozione di una regolamentazione europea che riduce tale periodo porrebbe il Paese in una posizione svantaggiosa rispetto ai centri di produzione europei a basso costo, secondo alcuni e alcune rappresentanti politiciCollegamento esterno.
Alcuni gruppi industriali sostengono che la Svizzera potrebbe essere vista come un’alternativa all’Europa se le aziende iniziassero a considerare l’UE come meno favorevole all’innovazione. “La Svizzera ha ora l’opportunità di rafforzare la sua buona reputazione come luogo di innovazione”, ha scritto Buholzer.
La bozza di revisione sarà ora discussa dal Parlamento e dal Consiglio europeo. Non è stata fissata alcuna scadenza per l’approvazione del disegno di legge e l’entrata in vigore.
Traduzione di Luigi Jorio

In conformità con gli standard di JTI
Altri sviluppi: SWI swissinfo.ch certificato dalla Journalism Trust Initiative





























Potete trovare una panoramica delle discussioni in corso con i nostri giornalisti qui.
Se volete iniziare una discussione su un argomento sollevato in questo articolo o volete segnalare errori fattuali, inviateci un'e-mail all'indirizzo italian@swissinfo.ch.